近期,中國科學院廣州生物醫藥與健康研究院發表了題為“USP7 restricts lineage potency in human embryonic stem cells through modulating mTOR activity”的研究論文。該研究揭示了一種限制人多能干細胞發育潛能的關鍵因子——去泛素化酶USP7,并闡釋其通過去除mTOR 蛋白上非經典K63多泛素化修飾,從而調控 mTOR 活性的全新機制。
細胞發育潛能限制
哺乳動物胚胎發育起始于受精卵,隨后經歷連續的譜系分化,最終形成完整個體。在早期胚胎發育中,細胞第一次命運分離發生在囊胚期,由全能性(totipotent)細胞分化為胚胎內的內細胞團(ICM)和胚外的滋養外胚層(TE)。ICM細胞雖保留分化為機體所有細胞類型的潛能,但向滋養外胚層等胚外組織(ExE)的發育潛能受到限制。的確,來源于ICM的體外培養人胚胎干細胞(human embryonic stem cells,hESCs)屬于多能性(pluripotent)細胞,展示有限的胚外組織潛能。這種從全能性向多能性的轉變標志著細胞譜系發育潛能的限制,然而其內在決定機制尚不明確。
刪除USP7,細胞潛能被釋放
研究人員首先發現,USP7缺陷的人胚胎干細胞表現出較強的單細胞存活能力。將這些細胞在擬胚體培養基中培養可形成擬胚體結構,隨后,當它們被轉入不含特定形態發生素的囊胚培養基(IVC)后,可自發形成類似囊胚的結構并表達胚外譜系(ExE)標志物,相比之下,野生型人胚胎干細胞無法呈現類似囊胚的結構也不表達胚外譜系標志物。進一步地,研究人員將這些類囊胚結構的聚集體進行貼壁培養后發現其能夠產生胚外的滋養層亞類細胞—絨毛外滋養層細胞和合體滋養層細胞,同時還形成了卵黃囊腔和羊膜腔典型胚胎腔結構。這些結果表明,USP7就像人胚胎干細胞發育潛能的“剎車”,限制了它向胚外組織發育,即敲除USP7解除了人胚胎干細胞的胚外譜系發育限制,并具備了模擬早期植入后胚胎發育、形成復雜胚胎樣結構的能力。
背后的機制:mTOR信號的調控
研究人員進一步探索USP7限制胚外潛能的作用機制,發現USP7敲除后,mTOR蛋白上的非經典K63泛素鏈無法被去除,從而導致mTOR蛋白磷酸化水平上升,并增強mTOR信號通路活性,這使得細胞內蛋白翻譯水平上調,尤其是多能性標志物的蛋白水平增加,最終導致人胚胎干細胞的胚外譜系限制被解除。簡而言之,USP7通過去除非經典的K63多泛素化而減弱mTOR活性,進而限制人胚胎干細胞的胚外發育潛能。
綜上,研究團隊鑒定了USP7介導的非經典K63泛素化去除這一關鍵內源機制,闡明了其如何限制人胚胎干細胞的胚外譜系發育潛能。同時,研究也暗示蛋白翻譯控制在早期細胞命運決定中發揮著至關重要的作用。這些發現不僅揭示了細胞發育潛能限制的多維調控,而且有助于優化模擬體外胚胎早期發育過程的培養體系。
潘光錦研究員和單永禮副研究員為論文的共同通訊作者,邢琦博士、李菲博士、碩士生馮瑤為論文的共同第一作者。該研究工作由中國科學院廣州生物醫藥與健康研究院、中國科學院香港創新研究院再生醫學與健康創新中心等單位合作完成,并得到了國家重點研發計劃、中國科學院、國家自然科學基金委、中國科學院青年創新促進會、廣東省及廣州市科技計劃等項目的資助。
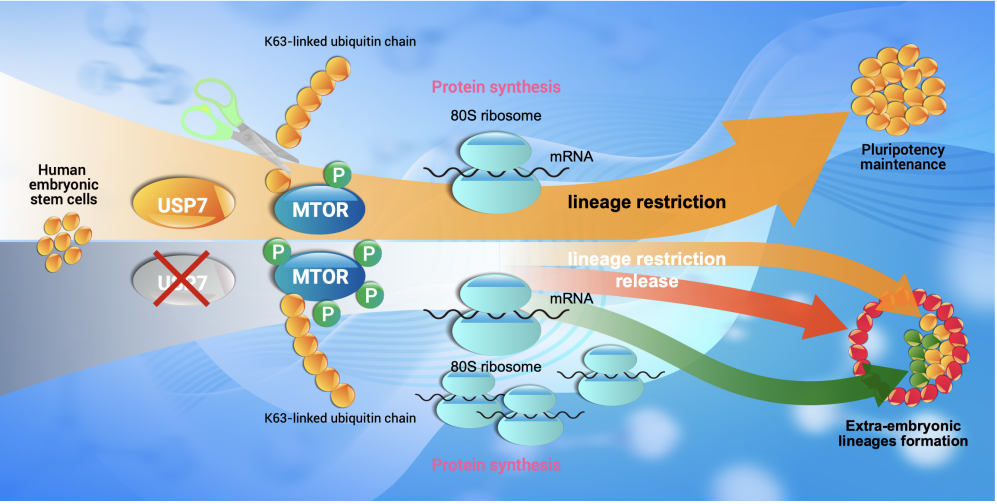
圖1 USP7通過調節mTOR信號通路調節胚胎干細胞發育潛能
附件下載:


